Ong Thế Duệ1, Đào Anh Sơn1, Lê Văn Truyền2, Kiều Thị Tuyết Mai3, Lê Hồng Minh2
1 Viện Chiến lược và Chính sách y tế
2 Trung tâm Nghiên cứu và Đánh giá Kinh tế Y tế
3 Trường Đại học Dược Hà Nội
I. TÓM TẮT
Mục tiêu:
Nghiên cứu này nhằm tổng quan hệ thống và so sánh hiệu quả, tính an toàn của Luseogliflozin so với Empagliflozin và Dapagliflozin ở bệnh nhân đái tháo đường type 2.
Phương pháp:
Nghiên cứu tiến hành theo khung PICOS, tìm kiếm tài liệu trên PubMed và Embase đến ngày 15/7/2024, bao gồm thử nghiệm có đối chứng ngẫu nhiên, tổng quan hệ thống và phân tích gộp so sánh Luseogliflozin với các thuốc ức chế kênh đồng vận chuyển natri-glucose 2 (SGLT2i) khác. Hai thành viên độc lập thực hiện sàng lọc và trích xuất dữ liệu, chất lượng nghiên cứu được đánh giá bằng bộ công cụ ROB-2 và AMSTAR-2.
Kết quả:
Tổng cộng 354 nghiên cứu được tìm thấy, trong đó 3 tổng quan hệ thống (233 thử nghiệm có đối chứng ngẫu nhiên, 155.106 bệnh nhân) đáp ứng tiêu chí lựa chọn. Chưa có thử nghiệm đối đầu giữa các thuốc. Cả 3 thuốc SGLT2i (Luseogliflozin, Dapagliflozin và Empagliflozin) đều vượt trội giả dược về kiểm soát glucose huyết tương và chuyển hóa. Luseogliflozin giảm HbA1c 0,49% (so với 0,74% của Dapagliflozin và 0,57% của Empagliflozin), giảm cân 1,68 kg (so với giảm 1,77-1,92 kg của Dapagliflozin và 1,93 kg của Empagliflozin), giảm huyết áp tâm thu/tâm trương 4,75/2,00 mmHg, tương đương 2 thuốc còn lại. Luseogliflozin cải thiện mỡ máu (giảm 18,69 mg/dL) và hạ acid uric (giảm 28,20 μmol/L) thấp hơn Dapagliflozin (giảm 36,99 mg/dL) và Empagliflozin (giảm 45,83 mg/dL). Về an toàn, Luseogliflozin không làm tăng nguy cơ nhiễm trùng sinh dục và có xu hướng ít biến cố niệu hơn, dù chưa đạt ý nghĩa thống kê.
Kết luận:
Luseogliflozin có hiệu quả tương đương các thuốc SGLT2i khác, với khả năng dung nạp tốt hơn ở nhóm bệnh nhân dễ gặp biến cố tiết niệu, sinh dục. Kết quả này là căn cứ khoa học để xem xét bổ sung thuốc vào danh mục bảo hiểm y tế, góp phần mở rộng tiếp cận điều trị và thúc đẩy cá thể hóa chăm sóc đái tháo đường type 2.
Từ khóa: Luseogliflozin, thuốc ức chế SGLT2i, đái tháo đường type 2, tổng quan hệ thống
II. ĐẶT VẤN ĐỀ
Đái tháo đường type 2 là một trong những bệnh không lây nhiễm phổ biến và có tốc độ gia tăng nhanh chóng trên toàn cầu. Theo Liên đoàn Đái tháo đường Thế giới (IDF), năm 2019 có khoảng 463 triệu người trưởng thành (20-79 tuổi) mắc bệnh đái tháo đường (ĐTĐ), con số này dự báo sẽ tăng lên 700 triệu người vào năm 2045 [1]. ĐTĐ gây ra nhiều biến chứng mạn tính nghiêm trọng như bệnh tim mạch, suy thận, mù lòa và cắt cụt chi, làm tăng gánh nặng y tế và tử vong sớm. Tại Việt Nam, tỷ lệ hiện mắc ĐTĐ ở người trưởng thành đã tăng từ khoảng 1-2% vào những năm 1990s lên 6% vào năm 2019. Đáng lưu ý, có tới gần 70% trường hợp ĐTĐ chưa được chẩn đoán, và trong số các bệnh nhân (BN) được chẩn đoán, chỉ có dưới 30% được quản lý thường xuyên tại cơ sở y tế [2]. Điều này cho thấy công tác kiểm soát bệnh còn nhiều hạn chế và gánh nặng bệnh tật ngày càng gia tăng. Trong điều trị ĐTĐ type 2, hiện nay có 7 nhóm thuốc chính đang được sử dụng, trong đó nhóm thuốc ức chế kênh đồng vận chuyển natri-glucose 2 (SGLT2i) được quan tâm đặc biệt nhờ cơ chế tác dụng mới, giúp kiểm soát glucose huyết tương độc lập với Insulin, đồng thời mang lại nhiều lợi ích ngoài hạ glucose huyết tương như giảm cân, hạ huyết áp (HA) và cải thiện chức năng tim, thận [3]. Theo Hướng dẫn chẩn đoán và điều trị ĐTĐ type 2 của Bộ Y tế, nhóm SGLT2i được khuyến cáo là lựa chọn ưu tiên cho các BN có bệnh tim mạch do xơ vữa, suy tim hoặc bệnh thận mạn [4]. Trong thực hành lâm sàng, Empagliflozin và Dapagliflozin đã được Quỹ Bảo hiểm y tế (BHYT) chi trả 70% tại các bệnh viện hạng I và II, tạo điều kiện tiếp cận cho BN [4].
Luseogliflozin (tên thương mại Lusefi®) là một thuộc nhóm SGLT2i, được cấp bằng độc quyền sáng chế và đưa vào Hướng dẫn điều trị bệnh ĐTĐ tại Nhật Bản, có cơ chế tác dụng tăng đào thải glucose qua thận, từ đó kiểm soát glucose huyết tương bền vững và giảm nguy cơ hạ glucose huyết tương. Các thử nghiệm lâm sàng quốc tế cho thấy Luseogliflozin giúp giảm HbA1c, cân nặng, HA và cải thiện các yếu tố nguy cơ tim mạch. Tuy nhiên, hiện nay thuốc chưa được đưa vào danh mục thuốc được BHYT chi trả tại Việt Nam, dẫn đến BN phải tự chi trả hoàn toàn và hạn chế khả năng tiếp cận thuốc trong cộng đồng.
Mặc dù đã có những nghiên cứu về hiệu quả của Luseogliflozin so với giả dược, nhưng hiện trong y văn chưa có nghiên cứu tổng quan hệ thống so sánh hiệu quả giữa Luseogliflozin và các thuốc cùng nhóm SGLT2i (bao gồm Empagliflozin, Dapagliflozin). Chúng tôi thực hiện nghiên cứu này nhằm tổng quan hệ thống và so sánh hiệu quả, tính an toàn của Luseogliflozin với Empagliflozin và Dapagliflozin ở bệnh nhân ĐTĐ type 2. Kết quả khoa học từ nghiên cứu này sẽ đóng vai trò quan trọng để cung cấp bằng chứng cho thực hành lâm sàng và làm căn cứ để xem xét bổ sung Luseogliflozin vào danh mục thuốc được BHYT chi trả.
III. ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
Nghiên cưu sử dụng khung PICOS (Population – Intervention – Comparator – Outcomes – Study design) để xây dựng câu hỏi nghiên cứu cho tổng quan hệ thống.
Bảng 1. Câu hỏi nghiên cứu diễn giải theo PICOS trong tổng quan hệ thống về hiệu lực, an toàn
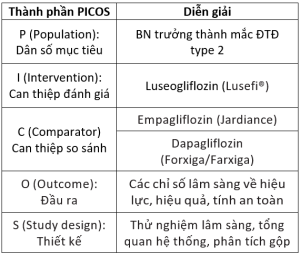
Nghiên cứu tiến hành tìm kiếm tài liệu trên hai cơ sở dữ liệu quốc tế có bình duyệt uy tín, bao gồm Med-line (truy cập qua PubMed) và Embase. Thời điểm tìm kiếm tài liệu là ngày 15/7/2024.
Chúng tôi xác định các từ khóa dựa trên nội dung câu hỏi nghiên cứu PICOS, trong đó không sử dụng từ khóa cho nội dung về đầu ra nghiên cứu và thiết kế nghiên cứu, nhằm tối đa hóa số lượng kết quả tìm kiếm. Chiến lược tìm kiếm cụ thể và kết quả tìm kiếm trên mỗi cơ sở dữ liệu được trình bày trong bảng 2.
Bảng 2. Tóm tắt chiến lược tìm kiếm trên các nguồn dữ liệu
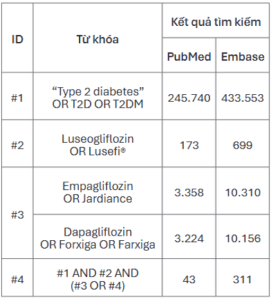
Quy trình lựa chọn nghiên cứu được tiến hành một cách hệ thống dựa trên bộ tiêu chí lựa chọn và loại trừ đã được xác định trước. Trước hết, các nghiên cứu được rà soát dựa trên tiêu đề và tóm tắt để loại bỏ những nghiên cứu không phù hợp. Trong trường hợp thông tin ở tiêu đề và tóm tắt chưa đủ căn cứ để đưa ra quyết định, nghiên cứu sẽ tiếp tục được rà soát toàn văn.
Để hạn chế sai số và nâng cao tính khách quan, hai thành viên nhóm nghiên cứu đã thực hiện độc lập toàn bộ quá trình sàng lọc (double screening) và tiến hành so sánh kết quả sàng lọc. Các điểm không đồng nhất được giải quyết thông qua đồng thuận giữa hai thành viên tiến hành sàng lọc hoặc xin ý kiến trưởng nhóm nghiên cứu.
Bảng 3. Tiêu chí lựa chọn và loại trừ nghiên cứu trong tổng quan hệ thống về hiệu lực, an toàn
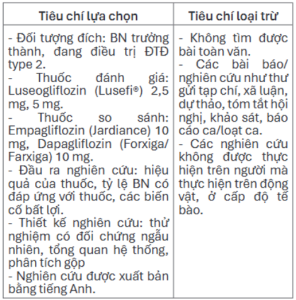
Trích xuất dữ liệu
Quy trình trích xuất dữ liệu được thực hiện một cách hệ thống nhằm bảo đảm tính chính xác và độ tin cậy. Các nghiên cứu được lựa chọn sau khi sàng lọc sẽ được tổng hợp theo các biểu mẫu trích xuất thông tin chuẩn hóa. Để hạn chế sai số, hai thành viên nhóm nghiên cứu đã thực hiện độc lập quá trình trích xuất dữ liệu (double data extraction) và tiến hành so sánh kết quả trích xuất. Các điểm không đồng nhất được giải quyết thông qua đồng thuận giữa hai thành viên tiến hành sàng lọc hoặc xin ý kiến trưởng nhóm nghiên cứu.
Các thông tin được trích xuất bao gồm: (1) Thông tin chung của nghiên cứu (tiêu đề, năm xuất bản, tên tác giả, tên thử nghiệm lâm sàng); (2) Đặc điểm chung về nghiên cứu (quốc gia hoặc khu vực, loại thiết kế nghiên cứu, thuốc đánh giá, thuốc so sánh, số lượng BN ở mỗi nhóm); (3) Thông tin chi tiết về đặc điểm BN, liều dùng và thời gian sử dụng thuốc; (4) Các chỉ số liên quan đến hiệu lực và hiệu quả điều trị; và (5) Các dữ liệu về tính an toàn của thuốc.
Đánh giá chất lượng nghiên cứu
Chất lượng các nghiên cứu được đánh giá bằng những công cụ chuẩn hóa quốc tế phù hợp, trong đó áp dụng bộ công cụ ROB-2 để đánh giá các nghiên cứu thử nghiệm lâm sàng và bộ công cụ AMSTAR-2 để đánh giá các nghiên cứu tổng quan hệ thống [5].
IV. KẾT QUẢ NGHIÊN CỨU
Tổng cộng 354 nghiên cứu được tìm thấy trên hai cơ sở dữ liệu (43 nghiên cứu từ Medline và 311 nghiên cứu từ Embase). Sau khi loại bỏ 26 nghiên cứu trùng lặp giữa hai cơ sở dữ liệu, 328 nghiên cứu được tiến hành rà soát tiêu đề và tóm tắt dựa trên các tiêu chí lựa chọn và loại trừ đã được xác định. Sau khi loại bỏ 298 nghiên cứu, 30 nghiên cứu tiếp tục được rà soát toàn văn.
Trong số 30 nghiên cứu được rà soát toàn văn, 27 nghiên cứu bị loại trừ. Cuối cùng, tổng cộng 3 nghiên cứu được đưa vào để tổng hợp và trích xuất thông tin, tất cả đều là nghiên cứu tổng quan hệ thống. Nhóm nghiên cứu không tìm thấy thử nghiệm lâm sàng so sánh trực tiếp Luseogliflozin và các thuốc SGLT2i khác.
Sơ đồ quá trình tìm kiếm và sàng lọc nghiên cứu theo hướng dẫn của PRISMA (Preferred Reporting Items for Systematic reviews and Meta-Analyses; Bảng kiểm báo cáo tổng quan hệ thống và phân tích gộp) được trình bày trong hình 1.
Hình 1. Sơ đồ PRISMA lựa chọn các nghiên cứu đưa vào tổng quan hệ thống về hiệu lực, an toàn
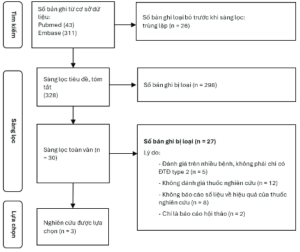
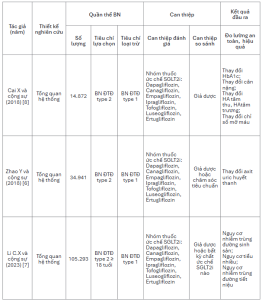
Tổng cộng có 3 nghiên cứu tổng quan hệ thống, dựa trên số liệu từ 233 thử nghiệm lâm sàng và 155.106 BN, được đưa vào phân tích. Kết quả cho thấy không có thử nghiệm lâm sàng nào so sánh đối đầu giữa Luseogliflozin và các thuốc SGLT2i khác, nhưng tất cả các thuốc SGLT2i đều cho thấy hiệu quả vượt trội so với giả dược. Cụ thể, về kiểm soát glucose huyết tương, cả 3 thuốc đều giúp giảm HbA1c có ý nghĩa thống kê, trong đó mức giảm lần lượt là 0,49% với Luseogliflozin, 0,74% với Dapagliflozin và 0,57% với Empagliflozin. Tương tự, cả 3 thuốc đều mang lại lợi ích giảm cân có ý nghĩa, với mức giảm trung bình từ 1,68 kg đến 1,93 kg [6-8].
Xét trên các chỉ số HA, Luseogliflozin, Dapagliflozin và Empagliflozin đều có hiệu quả giảm HA tâm thu và HA tâm trương so với giả dược. Mức giảm HA tâm thu dao động từ 1,68-1,93 mmHg, trong khi HA tâm trương giảm từ 2,00-4,44 mmHg. Về chỉ số mỡ máu, Luseogliflozin và Dapagliflozin đều cho thấy tác dụng giảm đáng kể so với giả dược, với mức giảm lần lượt là 18,69 mg/dL và 13,73 mg/dL. Ngoài ra, cả 3 thuốc cũng có tác dụng làm giảm nồng độ acid uric huyết thanh, trong đó Empagliflozin ghi nhận mức giảm mạnh nhất (45,83 μmol/L), tiếp theo là Dapagliflozin (36,99 μmol/L) và Luseogliflozin (28,20 μmol/L) [8].
Về tính an toàn, kết quả cho thấy Luseogliflozin không làm tăng nguy cơ nhiễm trùng đường sinh sản, trong khi Empagliflozin và Dapagliflozin có liên quan rõ ràng đến nguy cơ này. Đồng thời, nguy cơ tiểu nhiều và nhiễm trùng tiết niệu ở nhóm Luseogliflozin thấp hơn so với 2 thuốc còn lại, mặc dù sự khác biệt chưa đạt ý nghĩa thống kê. Như vậy, xét trên mặt bằng chung, Luseogliflozin có hồ sơ an toàn tương đương, thậm chí có ưu thế hơn ở một số biến cố bất lợi so với Empagliflozin và Dapagliflozin [6-8].
Bảng 4. Đặc điểm chung của các nghiên cứu
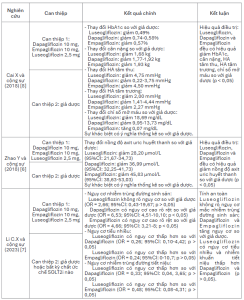
Bảng 5. Hiệu quả điều trị và tính an toàn
V. BÀN LUẬN
Nghiên cứu này là tổng quan hệ thống đầu tiên trong y văn đánh giá tính hiệu quả và an toàn của Luseogliflozin với Dapagliflozin và Empagliflozin trong điều trị ĐTĐ type 2 ở người trưởng thành. Nghiên cứu đã tiến hành tìm kiếm trên 2 cơ sở dữ liệu quốc tế uy tín, sử dụng chiến lược tìm kiếm mang tính mở, và tiến hành quy trình sàng lọc, trích xuất một cách hệ thống.
Dựa trên kết quả của 3 nghiên cứu tổng quan hệ thống, tổng hợp từ 233 thử nghiệm lâm sàng và 155.106 BN, cho thấy Luseogliflozin đạt hiệu quả kiểm soát đa yếu tố tương đương các SGLT2i khác. Cụ thể, so với giả dược, Luseogliflozin giảm HbA1c 0,49%, trong khi Dapagliflozin và Empagliflozin giảm lần lượt khoảng 0,74% và 0,57%; về cân nặng, mức giảm với Luseogliflozin là 1,68 kg so với giảm 1,77-1,92 kg của Dapagliflozin và 1,93 kg của Empagliflozin. Ở chỉ số HA, Luseogliflozin giảm HA tâm thu 4,75 mmHg và HA tâm trương 2,00 mmHg; các giá trị tham chiếu của Dapagliflozin là giảm 0,22-3,75 mmHg (HA tâm thu) và giảm 1,41-4,44 mmHg (HA tâm trương), còn Empagliflozin giảm khoảng 4,50 mmHg (HA tâm thu) và giảm 2,27 mmHg (HA tâm trương). Đối với rối loạn lipid, Luseogliflozin và Dapagliflozin đều giúp giảm lipid máu, lần lượt 18,69 mg/dL và 9,95-13,73 mg/dL. Ngoài ra, cả 3 thuốc đều có tác dụng hạ acid uric (có ý nghĩa thống kê), lần lượt là Luseogliflozin giảm 28,20 μmol/L, Dapagliflozin giảm 36,99 μmol/L, Empaglifloz-in giảm 45,83 μmol/L. Nhìn chung, hiệu quả của Luseogliflozin trong điều trị ĐTĐ type 2 phù hợp với yêu cầu điều trị hiện đại, nhấn mạnh tối ưu hóa đa mục tiêu (glucose huyết tương, cân nặng, HA, chuyển hóa), giúp cải thiện nguy cơ tim, thận dài hạn [9].
Về tính an toàn, dữ liệu tổng hợp cho thấy Luseogliflozin không làm tăng nguy cơ nhiễm trùng đường sinh sản so với giả dược (OR = 2,66; 95%CI: 0,43-19,67; p > 0,05), trong khi Dapagliflozin (OR = 6,53; 95%CI: 4,51-10,10) và Empagliflozin (OR = 4,66; 95%CI: 3,21-8,00) có nguy cơ tăng rõ. Đồng thời, biến cố bất lợi liên quan đến tiểu nhiều và nhiễm trùng tiết niệu ở nhóm Luseogliflozin có xu hướng thấp hơn Dapagliflozin (OR = 0,33; 95%CI: 0,04-3,65 cho nhiễm trùng tiết niệu) và Empagliflozin (OR = 0,48; 95%CI: 0,08-4,31), dù khác biệt chưa đạt ý nghĩa thống kê. Các số liệu này cho thấy Luseogliflozin có thể phù hợp với BN dễ gặp biến cố tiết niệu, sinh dục hoặc có tiền sử nhiễm trùng niệu. Tuy nhiên, một hạn chế quan trọng trong nghiên cứu tổng quan hệ thống này là thiếu dữ liệu so sánh trực tiếp giữa Luseogliflozin và Dapagliflozin/Empagliflozin, do trên thực tế chưa có các thử nghiệm lâm sàng đối đầu giữa các thuốc này. Trong tương lai, việc tiến hành các thử nghiệm lâm sàng so sánh trực tiếp giữa Luseogliflozin, Dapagliflozin và Empagliflozin nên được xem xét để làm rõ điểm mạnh, điểm yếu của từng thuốc, từ đó cung cấp căn cứ để lên phương án cá thể hóa điều trị cho mỗi BN ĐTĐ type 2.
VI. KẾT LUẬN
Luseogliflozin (Lusefi®) cho thấy hiệu quả kiểm soát đa yếu tố (HbA1c, cân nặng, HA, chuyển hóa) trong điều trị ĐTĐ type 2 và tính an toàn tương đương các thuốc cùng nhóm. Trên cơ sở này, các nhà hoạch định chính sách có thể xem xét bổ sung Luseogliflozin vào danh mục BHYT, góp phần mở rộng lựa chọn điều trị và hỗ trợ cá thể hóa phác đồ cho BN.
TÀI LIỆU THAM KHẢO
[1] Bergman M et al. International Diabetes Fed -eration Position Statement on the 1-hour post-load plasma glucose for the diagnosis of intermediate hyperglycaemia and type 2 diabetes. Diabetes Res Clin Pract, 2024, 209: p. 111589.
[2] Global, regional, and national burden of dia-betes from 1990 to 2021, with projections of prevalence to 2050: a systematic analysis for the global burden of disease study 2021. Lan-cet, 2023. 402 (10397): 203-234.
[3] Liu J et al. Effects of SGLT2i inhibitors on UTIs and genital infections in type 2 diabetes mel-litus: a systematic review and meta-analysis. Sci Rep, 2017, 7 (1): 2824.
[4] Bộ Y tế. Quyết định sô 5481/QĐ-BYT về việc ban hành tài liệu chuyên môn “Hướng dẫn chẩn đoán và điều trị đái tháo đường type 2”, Hà Nội, ngày 30 tháng 12 năm 2020.
[5] Shea B.J et al. AMSTAR 2: a critical apprais-al tool for systematic reviews that include randomised or non-randomised studies of healthcare interventions, or both. BMJ, 2017: j4008.
[6] Zhao Y et al. Effects of sodium-glucose co-transporter 2 (SGLT2i) inhibitors on serum uric acid level: A meta-analysis of random-ized controlled trials. Diabetes, Obesity and Metabolism, 2018, 20 (2): 458-462.
[7] Li C.X et al. Comparative safety of different sodium-glucose transporter 2 inhibitors in patients with type 2 diabetes: a systematic review and network meta-analysis of ran-domized controlled trials. Front Endocrinol (Lausanne), 2023, 14: 1238399.
[8] Cai X et al. No disparity of the efficacy and all-cause mortality between Asian and non-Asian type 2 diabetes patients with sodium-glucose cotransporter 2 inhibitors treatment: A me-ta-analysis. Journal of Diabetes Investigation, 2018, 9 (4): 850-861.
[9] Markham A, Elkinson S. Luseogliflozin: First Global Approval. Drugs, 2014, 74 (8): 945-950.
Tạp chí Y học Cộng đồng, tập 66, số chuyên đề 22, trang 306–312
